 |
為什麼要用碳十二來定原子量,別的不行嗎?(台北市/大理國中/二年級/林小弟) |
維尼哥哥:
事實上,在亞佛加厥定律提出之後,化學家是將一個氫原子的原子量定為1,以此為標準,其他元素再與氫做比較,求出原子量或分子量。
像一大氣壓、100℃時,一升的氫氣重0.0658公克,而氧重1.0460公克。因為氫分子、氧分子都由兩個原子組成,因此氧分子的分子量=(1.0460/0.0658)×
2=31.7933≒32。
到了西元1905年,國際原子量委員會決定以氧為原子量的標準,定其原子量為16,其他元素再與氧做比較。
但是,後來發現氧有三種同位素,質量數分別是16、17、18,因為同位素的組成會因時間、地點而有些微差別,因此,在西元1961年,國際純粹及應用化學聯合會(IUPAC)才決定以碳十二的質量作為原子量的標準,將一個碳十二原子質量的1/12定為原子質量單位(amu),1amu=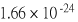 公克,依此標準,氧的原子量是15.9994。 公克,依此標準,氧的原子量是15.9994。
馬爺爺:
為什麼科學家最後選擇碳十二作為標準呢?那是因為週期表一百多個元素,光碳一個元素就形成了一個專門的領域
-
有機化學,是非常非常重要的生命元素,自然界到處都是碳;而當初訂定原子量標準時,有機化學正好當道,所以囉,時勢造英雄,碳十二就這樣成為原子量的標準啦!
|
|